1
冠状病毒概述

武汉知识产权研究会
电话:027-65692311
邮箱:xtc011@163.com
地址:湖北省武汉市洪山区民族大道特1号光谷资本大厦2009室
武汉东湖新技术开发区知识产权服务业协会
电话:027-87865011
邮箱:whfw011@163.com
地址:湖北省武汉市洪山区民族大道特1号光谷资本大厦2009室
二〇二〇年十月六日
防疫疫苗与知识产权策略
江慧
(北京众达德权知识产权代理有限公司生化领域专利代理人)
摘要
本文对冠状病毒疫苗的有关专利申请/专利进行了统计,发现主要涉及亚单位疫苗、合成肽疫苗、DNA疫苗、活载体疫苗、减毒疫苗、灭活疫苗、联苗等类别。其中亚单位疫苗所占比例最多,达21%,其次为合成肽疫苗、核酸疫苗、活载体疫苗。其中毒株的获得为制备灭活疫苗或减毒疫苗提供了基础。并对目前已进入临床实验阶段的2019新型冠状病毒肺炎疫苗情况进行了统计。最后提出了防疫疫苗的知识产权策略。
关键词
冠状病毒疫苗;知识产权
引言:随着全球新型冠状病毒感染人数不断攀升,我国科研工作者正在针对性的有效药物开发和疫苗研制工作。目前全球多家科研机构和制药公司致力于研发新型冠状病毒疫苗和治疗药物。本文对冠状病毒疫苗的有关专利申请/专利进行了统计,并列出具有代表性的冠状病毒疫苗,可能会对本次的新型冠状病毒疫苗的研发有一定的借鉴意义,同时对目前已进入临床实验阶段的2019新型冠状病毒肺炎疫苗情况进行了统计,提出了防疫疫苗的知识产权策略,对后续开发的有自主知识产权的疫苗进行国际国内外市场的布局,实现知识产权全方位保护具有一定的借鉴意义。
1
冠状病毒概述
冠状病毒是一种含有大约30,000个碱基的正极性单链RNA的病毒, 其RNA在宿主细胞的细胞质中复制;其基因组的5’端有帽结构,3’端 包含多聚腺苷酸尾部。该病毒包于包膜中,并在表面含有称为刺 (spicule)的突起结构。该基因组从其5’端到3’端包括下述的开放读码框或ORF:对应于转录-复制复合物的蛋白的ORF1a和ORF1b,对应于结构蛋白S、E、M 和N的ORF-S、ORF-E、ORF-M和ORF-N。它还包括对应于编码未知功能 蛋白的ORF:位于ORF-S和ORF-E之间并与后者重叠的区域;位于ORF-M 和ORF-N之间的区域;包括于ORF-N的区域[1]。
S蛋白是一种膜糖蛋白(200-220kDa),其存在于从病毒包膜表面形 成的刺或刺突的形式中。它在病毒附着于宿主细胞的受体并诱导病毒包 膜和细胞膜相融合的过程中起作用[2]。
小包膜蛋白(E),也被称为sM(smallmembrane),是一种约10kDa 大小地非糖基化跨膜蛋白,是病毒体中含量最少的蛋白质。它在冠状病 毒在内质网和高尔基体的中间区域的出芽过程中起了重要作用[3]。
M蛋白或基质蛋白(25-30kDa)是一种含量较多的膜糖蛋白,它通过M/E相互作用整合至病毒颗粒中,而S蛋白通过S/M相互作用结合到 病毒颗粒中。M蛋白看来对于冠状病毒的成熟和对于病毒颗粒装配位点的决定十分重要。
N蛋白或核壳蛋白(45-50kDa)是冠状病毒结构蛋白中最保守的, 它对于基因组RNA的壳体化和支配其与病毒体结合都是必需的。该蛋白可能还参与了RNA的复制。SARS的N蛋白可以和患者血清发生反应,并且表达SARS的N蛋白的DNA疫苗也可以诱导小鼠产生抗体反应。另有研究显示鼻内接种N蛋白的通用T细胞表位的载体疫苗后,可诱导气道记忆CD4+T细胞应答,对SARS-CoV和MERS-CoV均产生保护反应,提示针对N蛋白的通用保守T细胞表位是开发泛冠状病毒疫苗的潜在策略[4]。
新型冠状病毒属于Beta冠状病毒属,SARS病毒的S-蛋白和MERS病毒S-蛋白分别通过与人的ACE2蛋白互作结合来感染人的呼吸道上皮细胞。研究表明新型冠状病毒也是通过S-蛋白与人ACE2互作的分子机制,来感染人的呼吸道上皮细胞[5]。
上述内容,提示2019-nCoV的S蛋白、N蛋白(N蛋白的T和B细胞表)、M蛋白是疫苗开发的潜在靶标,目前在研的新冠疫苗也主要以S蛋白为靶点设计开发。
2
关于冠状病毒疫苗的专利申请/专利状况
2.1申请趋势
截止2020年04月08日,于incopat检索网站,检索式TIAB=(冠状病毒 AND 疫苗)主要针对中国专利,检索到有关冠状病毒疫苗专利申请/专利共105件,年申请趋势详见图1。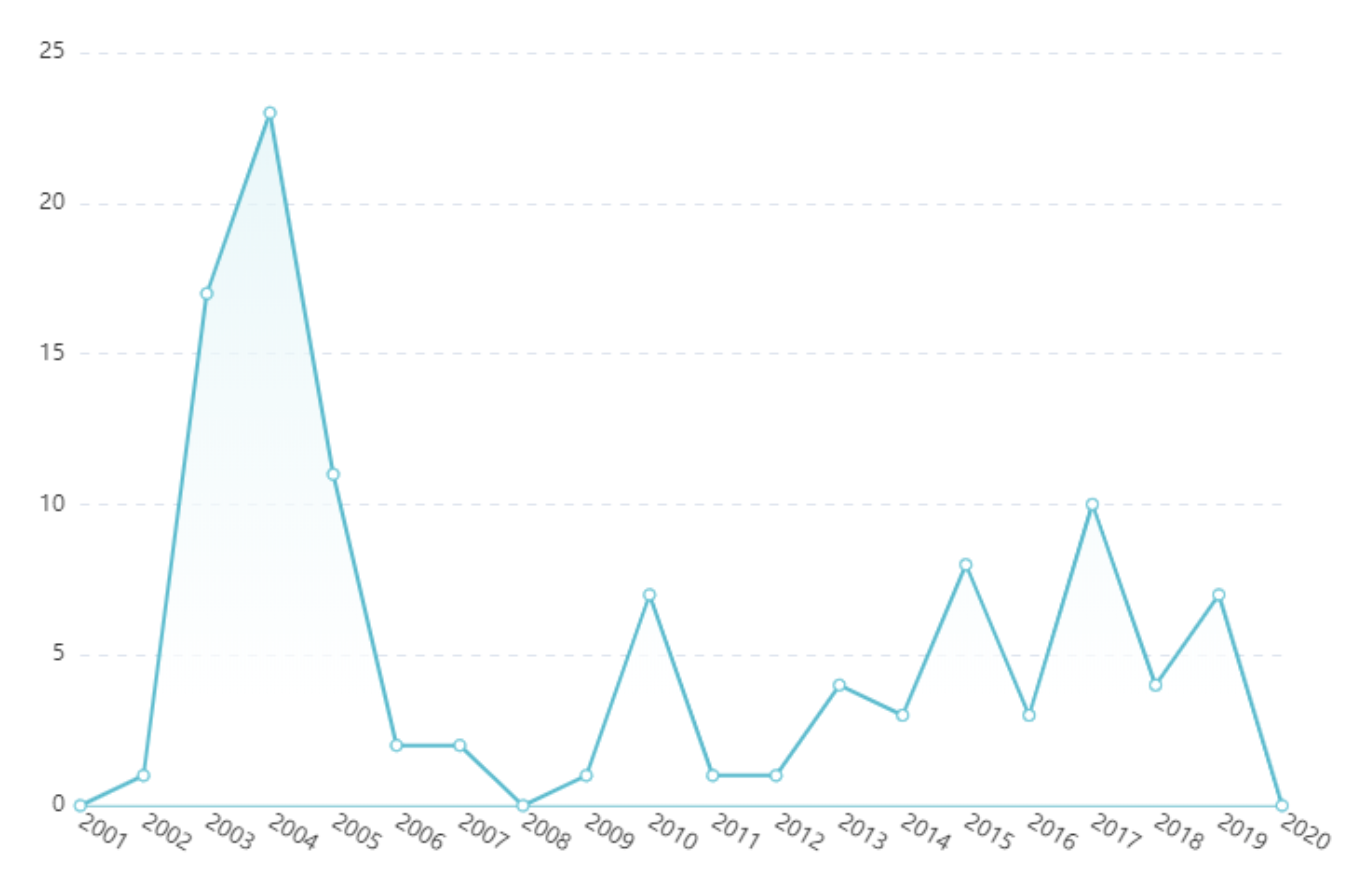
图1-冠状病毒疫苗专利申请/专利之申请趋势
2.2冠状病毒疫苗的专利申请/专利之法律状态
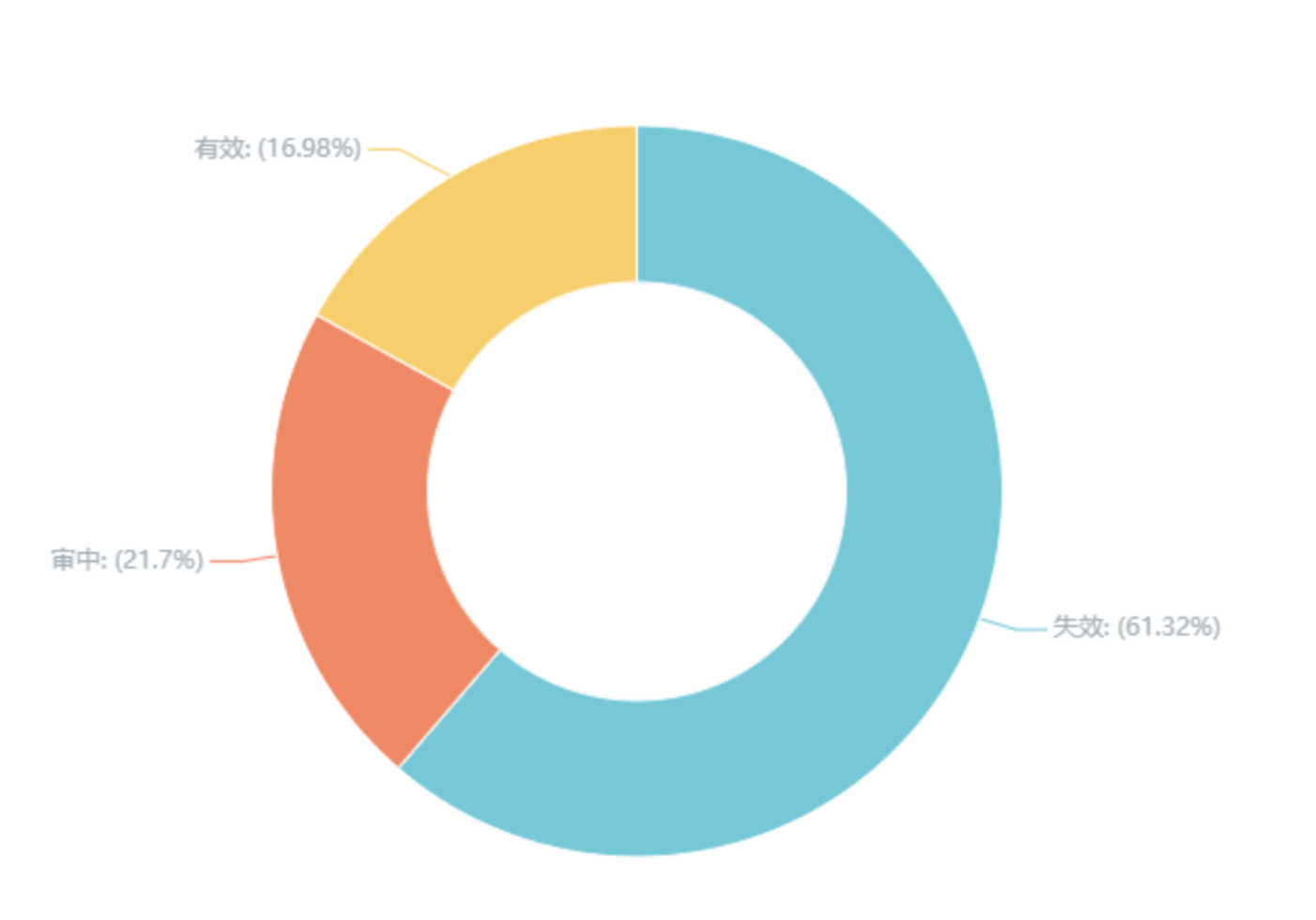
图2 冠状病毒疫苗专利申请/专利之法律状态
注:法律状态“审中”是指专利申请仍处于审查状态,尚未获得专利权;法律状态“失效”包括审查中失效和终止失效,其中审查中失效指专利申请在审查过程中,由于申请人对官方的来文未做回应或申请档缺陷未被消除等情況而导致的专利申请权丧失的情形;“终止”失效是指专利权人在未按规定缴纳年费或者届满等情況下致使专利权丧失的情形。法律状态“有效”是指取得了专利权後专利权人定期缴纳了年费,以维持专利权有效的状态。
2.3申请人排名
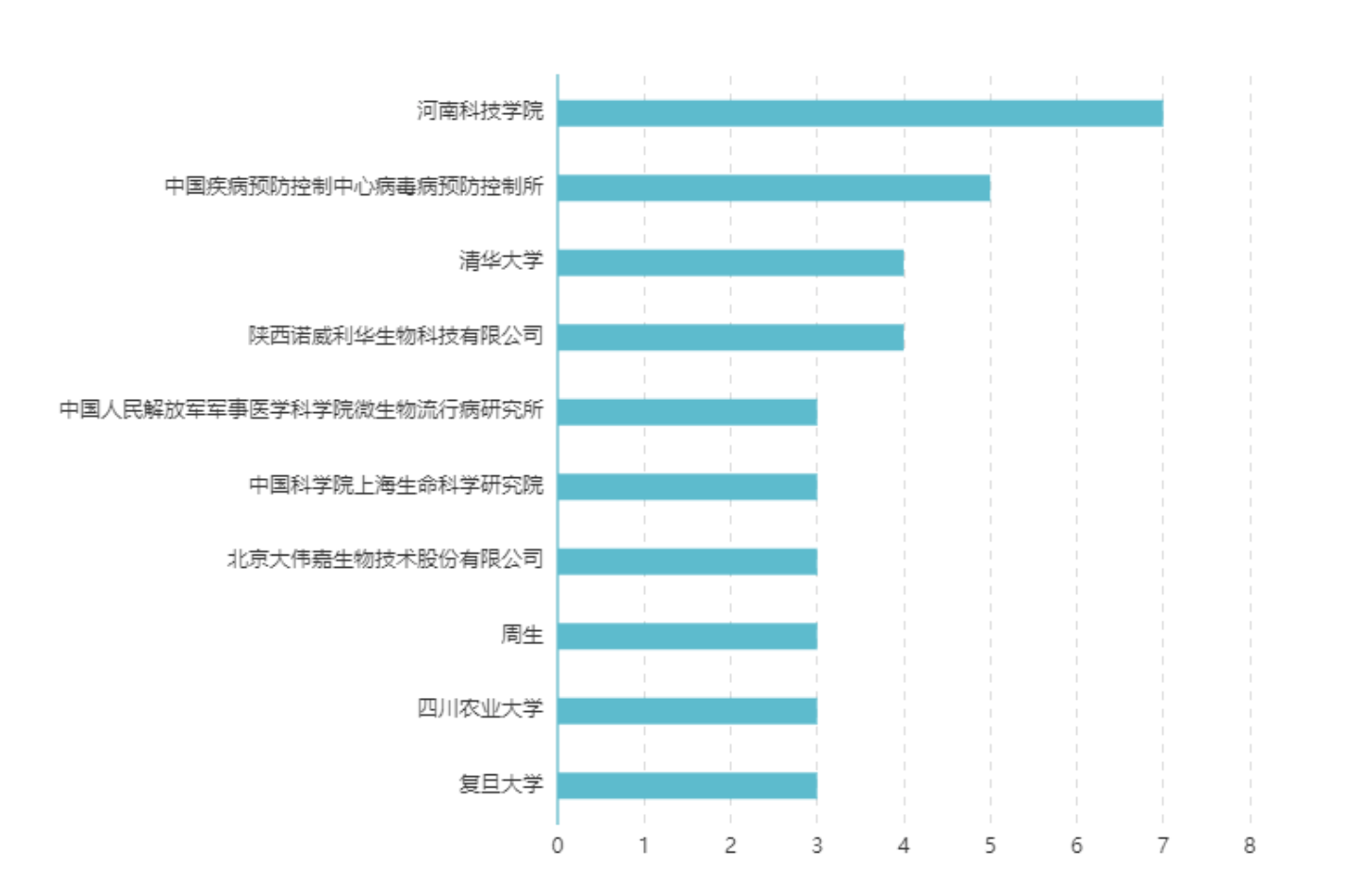
图3 冠状病毒疫苗专利申请/专利之申请人排名
(1)冠状病毒疫苗的专利申请/专利涉及亚单位疫苗、合成肽疫苗、DNA疫苗、活载体疫苗、减毒疫苗、灭活疫苗、联苗等类别。其中亚单位疫苗所占比例最多,达21%,其次为合成肽疫苗、核酸疫苗、活载体疫苗。其中毒株的获得为制备灭活疫苗或减毒疫苗提供了基础。
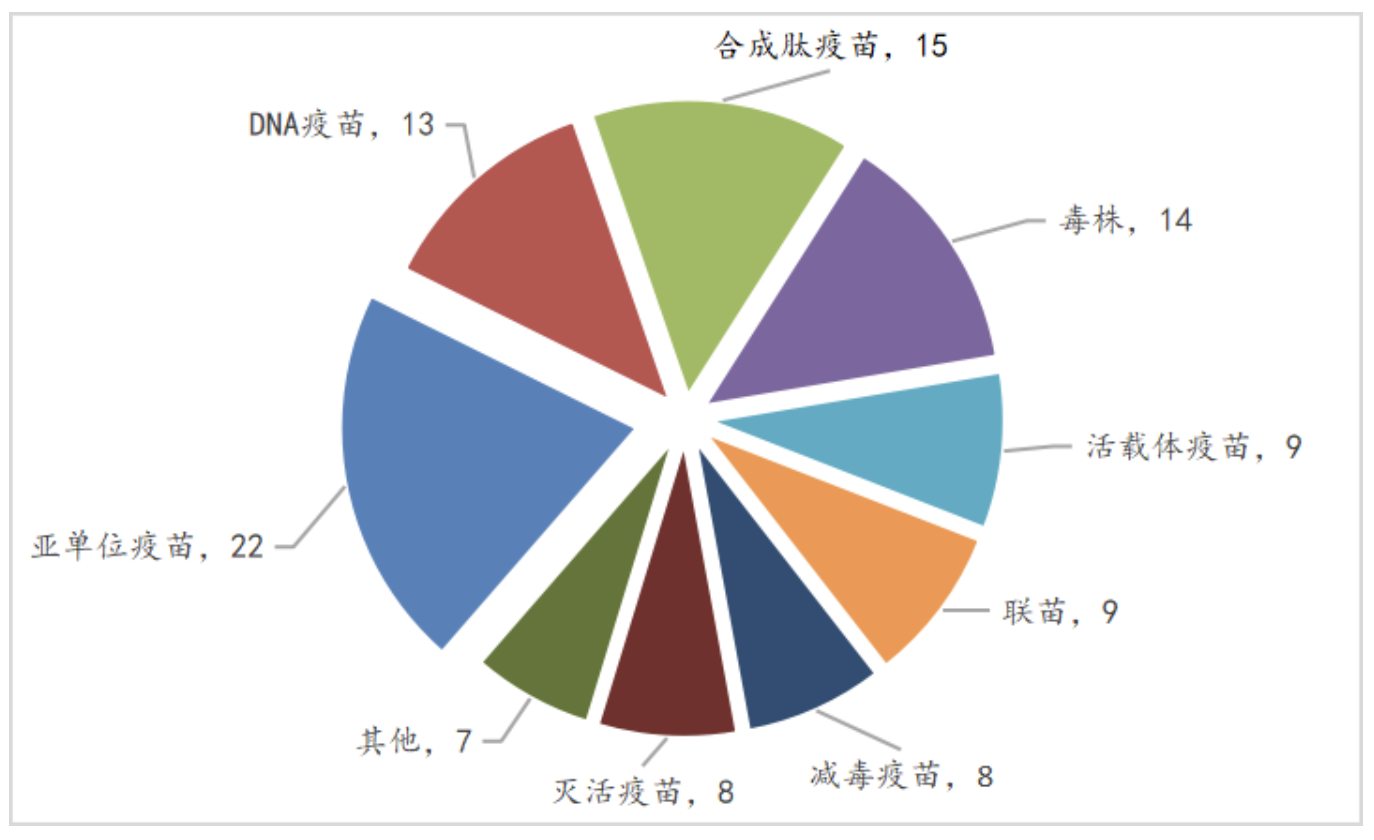
图4 冠状病毒疫苗专利申请/专利的大类别分布
表1 冠状病毒疫苗专利申请/专利所涉及类别
类别 | 类别说明 | 数量 |
灭活疫苗 | 使用化学灭活剂将病原微生物温和地杀死,但仍保持其免疫原性 | 8 |
亚单位疫苗 | 为重组表达能诱导保护性免疫应答的目的抗原的疫苗,不含病原体核酸, | 22 |
活载体疫苗 | 又称重组载体疫苗,是将有效的目的抗原的编码基因导入活载体(无或弱毒的细菌或病毒株)中,构建重组菌株;目的基因可随重组菌株在宿主体 内的增值而大量表达,从而诱发相应的免疫保护作用。 | 9
|
DNA疫苗 | 将一种或多种目的抗原的编码基因克隆岛真可质粒表达载体上;再将重组质粒直接注入到体内,在宿主细胞内表达目的蛋白,诱发特异性免疫应答 | 13 |
RNA疫苗 | RNA疫苗由信使RNA链组成。它们被注射到体内,通常是脂质纳米颗粒包裹。它们与细胞融合。一旦进入细胞,RNA序列被核糖体翻译成蛋白质或蛋白质的一部分。与DNA不同,RNA不能被整合到宿主基因组中,并导致突变。 | TW201729835A 呼吸道病毒RNA疫苗 |
合成肽疫苗 | 合成肽疫苗也成为表位疫苗,是用化学合成法人工合成类似于抗原决定簇的小肽(约20~40个氨基酸)并将其连接到大分子载体上,再加上佐剂制成的疫苗,通常由多个B细胞抗原表位和T细胞抗原表位共同组成。 | 15 |
联苗 | 由两种以上的细菌(或病毒)联合制成的疫苗一次免疫可达到预防几种疾 病的目的。 | 9 |
毒株 | 自然界筛选的毒株,或通过反向遗传学系统建立得到的毒株 | 14 |
其他 | 包括:适宜分泌表达病原微生物(冠状病毒)抗原的大肠杆菌-分枝杆菌穿梭载体质粒;SARS康复者血液淋巴细胞中差异表达基因的cDNA文库;提高抗原免疫活性的佐剂(包括新的人或动物热休克蛋白gp96和hsp108 或hsp70全长分子或其氨基端片段);优化病毒复制的培养基;优化的制备灭活疫苗和/或减毒活疫苗的方法,在宿主细胞中过表达胶质瘤抑癌候选基因2,并用灭活疫苗和/或减毒活疫苗生产用毒株接种宿主细胞,培养细胞,收获病毒液。 | 7 |
2.5有代表性的专利申请内容的简要介绍
(1)亚单位疫苗
CN106928326A表达S蛋白的RBD作为亚单位疫苗。具体地公开了一种基于二聚化的受体结合区亚单位的冠状病毒疫苗,属于医药技术领域。本发明通过杆状病毒体在昆虫细胞里表达MERS-CoV蛋白的RBD(E367-Y606)区域和ARS-CoV的RBD(R294-F515),使得RBD可通过S蛋白自身603位的半胱氨酸残基形成二聚体或者通过S蛋白自身512位的半胱氨酸残基形成二聚体,分别使用纯化的RBD蛋白二聚体和单体对Balb/c小鼠进行免疫。
CN1597964A:高效表达和纯化重组SARS 病毒M蛋白作为亚单位疫苗。
CN1552731A:表达的SARS冠状病毒N蛋白作为亚单位疫苗。
(2)核酸疫苗
CN1562366B:它包含SARS相关冠状病毒S 基因和真核表达质粒,能诱导机体同时产生针对引起非 典传染病的SARS冠状病毒S蛋白的特异性体液免疫和细胞免疫。
CN1449827:公开了一种SARS病毒DNA疫苗pVPH,由分泌型HE蛋白抗原决定簇编码 序列HE-P和真核表达载体构成;所述HE (hemagglutinin-esterase)即红细胞凝集素酯酶,为冠状病毒的主要抗原之一,可与 特异性受体结合,凝集血红细胞。
(3)活载体疫苗
CN105273067A:公开了一种编码MERS-CoV棘突蛋白的重组41型腺病毒载体疫苗。本发明首先合成了中东呼吸综合症冠状病毒(MERS-CoV)棘突蛋白(S)的编码基因,将其插入pSh41-CMV载体,获得重组质粒pAd41-MERS-S;转染HEK293细胞,获得拯救病毒Ad41-MERS-S。
CN105543248A:公开了一种高效表达MERS-CoVS蛋白的重组5型腺病毒载体疫苗。本发明首先优化合成了中东呼吸综合症冠状病毒(MERS-CoV)棘突蛋白(S)的编码基因,将其插入pShuttle-CMV载体,获得重组质粒pAd5-MERS-S;转染HEK293细胞,获得拯救病毒Ad5-MERS-S。
CN101007168:公开了一种SARS疫苗及其制备方法。该SARS疫苗是以杆状病毒为载体,在其表面展示有SARS冠状病毒S蛋白胞外区的重组杆状病毒。其制备方法包括以下步骤:1)构建SARS冠状病毒S蛋白胞外区的杆状病毒表面展示载体;2)将SARS冠状病毒S蛋白胞外区的杆状病毒表面展示载体转化含有杆状病毒基因组质粒Bacmid的感受态细胞,得到重组杆状病毒基因组质粒;3)将重组杆状病毒基因组质粒转染昆虫细胞,对培养上清中的重组杆状病毒粒子进行纯化后,得到SARS疫苗。
3
目前已进入临床实验的2019-nCoV疫苗
对2020.04.08号之前已进入临床实验阶段的2019新型冠状病毒肺炎疫苗情况进行统计,如表2所示。
表2 -进入临床实验阶段的2019新型冠状病毒肺炎疫苗情况
疫苗类型 | 进入临床实验的2019新型冠状病毒肺炎疫苗 |
活载体疫苗 | 1、Ad5-nCoV,是基于5型复制缺陷腺病毒作为表达2019-nCoV spike蛋白的载体。由中国军事医学科学院生物技术研究所和天津Cansino生物技术有限公司研发,目前处于2019新型冠状病毒肺炎的临床一期试验阶段,临床试样注册号:NCT04313127。 2、ChAdOx1 nCoV-19,是牛津大学开发的,基于猴腺病毒载体的包含COVID-19病毒表面突触蛋白(Spike)的疫苗,目前处于2019新型冠状病毒肺炎的临床一期试验阶段段,临床试样注册号:NCT04324606。 |
RNA疫苗 | mRNA-1273,是一种脂质纳米颗粒信使核糖核酸(mRNA)疫苗,编码新型冠状病毒的Spike (S)蛋白,由美国国家过敏和传染病研究所和Moderna公司开发。目前处于治疗新型冠状病毒肺炎的一期临床试验,临床试验注册号: NCT04283461。 |
亚单位疫苗 | 病原体特异性人工抗原是深圳市免疫基因治疗研究院开发的一种疫苗,目前处于治疗和预防新型冠状病毒肺炎的临床一期试验阶段,临床试验注册号: NCT04299724. |
4
防疫疫苗的知识产权策略
对防疫疫苗的相关专利进行多主题进行专利布局,以多件不同主题的专利进行布局形成专利壁垒,包括针对不同的抗原、选用不同的载体,选用不同的疫苗类型等核心专利进行布局,同时可对优化病毒复制的培养基、减毒的方法、佐剂的选择等外围专利进行布局。多主题专利布局不仅可以形成专利群扩大保护范围而且可以延长保护期限。
在具备单一性的前提下也可对同一件专利中多主题布局,以专利CN1981032为例,其独立权利要求的布局包括毒株、引物对、探针、重组克隆和/或表达载体、细胞、单克隆抗体、检测试剂、免疫复合物、检测试剂盒。
参考文献
